por Ronald Estrada Seminario
Para comprender las distintas patologías gástricas es necesario entender el rol que cumplen la barrera defensiva y el equilibrio que tiene que haber entre ésta y los agentes agresores.
Es importante conocer que las diversas patologías gastroduodenales no siempre se acompañan de hiperclorhidria, hecho fundamental para aplicar la terapéutica correcta.
En este capítulo se tratará de hacer una revisión breve sobre la conformación de la barrera defensiva gástrica y como los distintos componentes interactúan para ser más efectiva la protección.
La diferencia de pH que existe entre superficie del moco gástrico(pH=1) y el de la superficie del epitelio de revestimiento(pH=7) es necesario para evitar la retrodifusión de iones que es lo que produce la lesión tisular.
El bicarbonato es secretado por células superficiales que son ricas en anhidrasa carbónica; estas células también secretan mucinas por lo que el gel mucoso que cubre el epitelio gástrico tiene un pH=7.
El hidrógeno retrodifunde muy lentamente a través del gel hacia el epitelio y en su camino hacia la superficie epitelial se encuentra con el bicarbonato que lo transforma en H2O y CO2. el mismo camino sigue la pepsina que al encontrarse con un pH=7 se inactiva.
Los factores que regulan la secreción gástrica de bicarbonato no están del todo claro, pero hay dos mecanismos conocidos:
La estimulación vagal aumenta la secreción gástrica de bicarbonato por vías colinérgicas.
Los análogos de las prostaglandinas (E2) aumentan la secreción gástrica de bicarbonato y también actúan sobre la microcirculación aumentando el flujo sanguíneo.
Además del bicarbonato, el moco juega un papel importante en la constitución de la barrera defensiva gástrica.
El gel mucoso existe en dos formas físicas, una delgada capa de mucina que se adhiere firmemente a la superficie mucosa gastroduodenal (moco adherente) y mucina que se mezcla con el líquido luminal y puede ser lavada de la superficie mucosa (moco soluble).
Esta mucina proporciona lubricación superficial y una capa de agua no revuelta lo cual enlentece la difusión de protones hacia la mucosa (ver figura 1).
El factor d crecimiento epidérmico, secretado por las glándulas de Brünner, que controla el ADN a través del índice mitótico celular, permitiendo que normalmente en el lapso de 4 días sea reemplazado todo el epitelio gástrico.
La SAME, constituyente biológico de la célula, después del ATP es el más importante, ya que activa el ADN, forma poliaminas, aumenta los sulfhidrilos y en particular el moco gástrico, o sea las glicoproteínas. La
SAME es un citoprotector superior a las prostaglandinas, hecho bien comprobado frente a poderosos agresores como el etanol absoluto y la aspirina.
Agentes agresores
Drogas y medicamentos
La aspirina es una de las principales agresoras de la mucosa gástrica porque bloquea las prostaglandinas que son las responsables de regular la microcirculación y secreción de bicarbonatos, factores necesarios para mantener el gradiente de pH y así evitar la retrodifusión de protones.
La aspirina además por acción directa destruye las células epiteliales liberando histaminas lo que aumenta la congestión y posterior hemorragia gástrica. La ingesta de dos comprimidos de aspirina produce una pérdida de 4 a 8 ml de sangre, medida por volemia y sangre oculta en materia fecal. Todos los analgésicos no esteroides provocan la aparición de sangre oculta en la materia fecal.
El alcohol en dosis bajas (250ml/día) tiene acción citoprotectora, pero en dosis mayores produce necrosis celular directa.
Los corticoides retardan el índice mitótico celular (envejecimiento celular) degradan el moco gástrico y bloquean las prostaglandinas facilitando la retrodifusión de protones.
Sales biliares y jugos pancreáticos
La lecitina más la fosfolipasa A forman la isolecitina la cual a un pH ácido es necrotizante de la mucosa gástrica; es lo que se conoce como gastritis alcalina.
Irritantes gástricos
El café aumenta la secreción ácida y relaja el esfínter esofágico inferior lo mismo que el té y el mate.
El tabaco disminuye el tonismo del esfínter esofágico inferior favoreciendo el reflujo gastroesofágico y produce además hipotonía del esfínter pilórico facilitando el reflujo duodeno pancreático (lecitina).
La urea que se elimina por la mucosa gástrica produce congestión y hemorragia la cual responde solamente a la disminución de uremia por medio de la hemodiálisis.
Alergia alimentaria
Es muy frecuente; las gastritis aftosas y las erosivas crónicas responden a esta etiología. Mención aparte como entidad es la gastroenteritis eosinofílica.
Bacterias
Las intoxicaciones alimentarías, que habitualmente dan gastroenteritis, se acompañan de gastritis microbianas. Lo mismo ocurre con la gastritis moniliásica en la cual es habitual el muguet bucal.
Endotoxinas
Actúan provocando marcada congestión gástrica, lo cual, sumado a cualquier agente agresor, produce la gastritis hemorrágica característica del shock endotóxico.
CLASIFICACION DE GASTRITIS
Las clasificaciones de gastritis tienen dos objetivos diferentes. El primero es proporcionar una descripción general rápida de la patología (es decir las anormalidades y el grado de severidad endoscópico e histológico). El segundo objetivo se refiere a la patogenia asociada o las asociaciones clínicas o a ambas cosas (asociadas a helicobacter pylori).
De acuerdo a la evolución pueden ser agudas y crónicas.
Las gastritis agudas se caracterizan por su aspecto congestivo y por la diapédesis transepitelial y transcrípticas de los polinucleares.
La gastritis crónicas pueden ser superficial con infiltrado linfoplasmocitario del tercio superior de la mucosa, crónica atrófica donde el infiltrado toma toda la mucosa y atrófica gástrica que se caracteriza por disminución del espesor de la mucosa del estómago con ausencia total de las glándulas fúndicas que se acompañan habitualmente de metaplasia intestinal.
En el intento de simplificar y facilitar el entendimiento del alumno se va a superponer las distintas clasificaciones y luego se desarrollará detalladamente las más importantes.
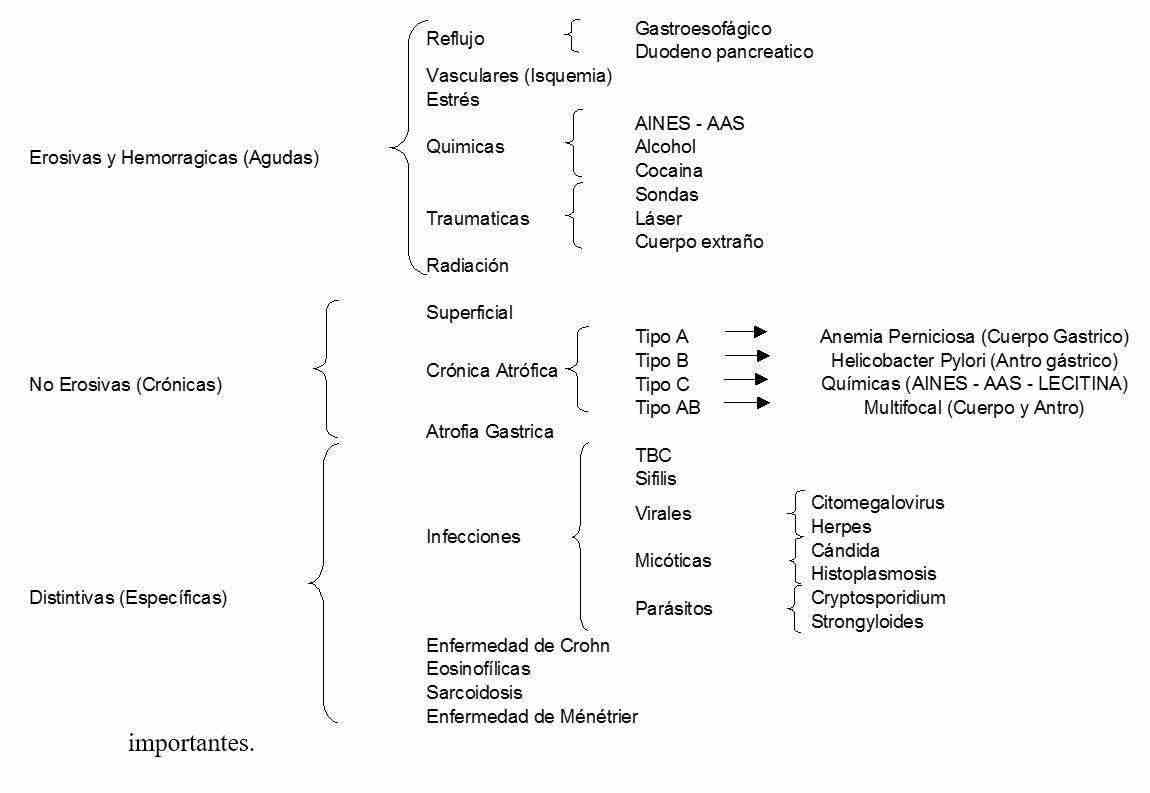
GASTRITIS EROSIVAS Y HEMORRÁGICAS
Las lesiones erosivas o hemorrágicas se visualizan endoscópicamente y en general no se biopsia, a menos que se sospeche un tipo distintivo de gastritis como infección o enfermedad de Crohn.
La erosión es la rotura superficial que no atraviesa la muscular de la mucosa hacia la submucosa. La endoscopia revela lesiones generalmente múltiples con bases blancas y radiadas por un halo de eritema, cuando las erosiones han sangrado recientemente su base puede verse negra.
Una hemorragia subepitelial se ve con el aspecto de petequias o estrías y parches de color rojo brillante ubicadas en la mucosa o en la submucosa.
Las causas de gastritis erosivas – hemorrágicas son el alcohol, los AINES, sondas nasogástricas, isquemia, reflujo duodeno pancreático, reflujo gastroesofágico (inflamación de la región del cardias)
GASTRITIS NO EROSIVAS
En la gastritis no erosiva el diagnóstico es histológico, el aspecto endoscópico no predice su presencia y el patrón histológico es inespecífico.
Existen tres patrones de gastritis atrófica
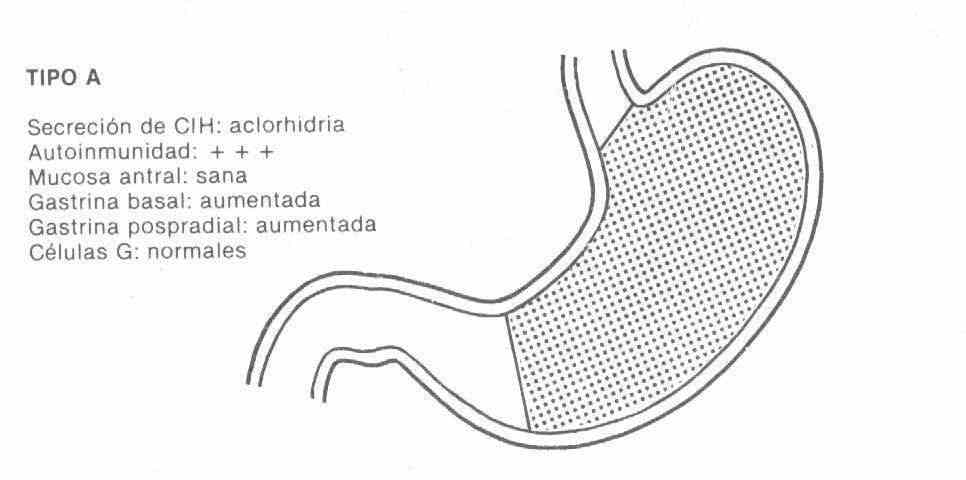
TIPO A: se asocia con una anemia perniciosa, los pacientes afectados tienen anticuerpos contra la bomba de protones, el pepsinógeno y el factor intrínseco, la pérdida de función secretora comienza con el ácido, sigue con el pepsinógeno y finalmente con el factor intrínseco, por lo que la anemia perniciosa es un marcador de la forma terminal más severa de la gastritis atrófica tipo A.
Se localiza en el fondo gástrico, el antro está sano. Tiene elevados niveles de gastrina por falta de inhibición ácida, ya que presenta una aclorhidria con debito ácido cero.
Esta gastritis tipo A se halla asociada a otras enfermedades inmunitarias como la tiroiditis del hashimoto, el hipotiroidismo, la diabetes, el vitíligo.
Es de escasa frecuencia en nuestro medio y en ocasiones puede progresar a la malignidad.
TIPO B: La causa más importante y habitual es el Helicobacter Pylori, comienza en el antro y se extiende progresivamente hacia el cuerpo y el cardias.
Al ser infecciosa se caracteriza por el gran infiltrado inflamatorio predominio polinuclear e incluso presenta microabcesos crípticos.
Secreción CIH: normal o aumentado
Autoinmunidad: Anticuerpos Anticélulas G (-)
Mucosa antral: enferma
Gastrina basal: normal ó aumentada
Gastrina postprandial: normal ó aumentada
Células G: disminuidas
Los niveles de gastrina y secreción ácida son alrededor de un 35 a un 45% más elevados en los individuos normales infectados por Helicobacter Pylori que en los controles no infectados.
Debido a la importancia de la presencia del Helicobacter Pylori en esta patología se harán algunas consideraciones al respecto
Helicobacter Pylori es un microorganismo espiralado gram (-), sumamente móvil, microaerófilo y de crecimiento lento, cuya característica bioquímica más notables es la producción de ureasa.
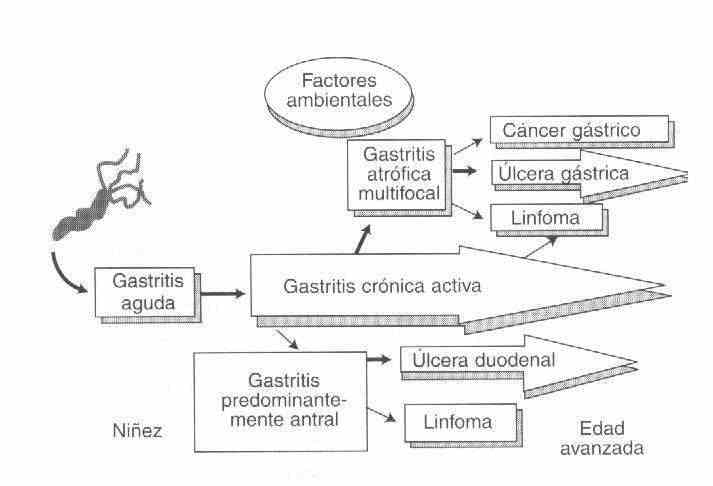
El Helicobacter Pylori puede colonizar solo epitelio de tipo gástrico, es decir el estómago y las áreas de metaplasia gástrica fuera del estómago. El reemplazo de las células columnares de las vellosidades duodenales por epitelio de tipo gástrico se presenta en el 90% de los pacientes con úlcera duodenal, lo que permite al Helicobacter Pylori colonizar el bulbo y producir una inflamación crónica duodenal.
La vía de infección puede ser fecal oral u oral, gastro oral (Por endoscopio inadecuadamente desinfectados), por agua o alimentos contaminados.
Además de la gastritis tipo B existen otras patologías asociadas al Helicobacter Pylori como ser Ulcera Gástrica, Ulcera Duodenal, Carcinoma Gástrico.
Linfoma no Hodking – Linfoma Malt.
TIPO C: es la gastritis química provocada por la ingesta de AAS, AINES, Alendronato, o la lecitina del reflujo biliar. Tiene escasa o no tiene infiltrado inflamatorio.
TIPO AB: es multifocal con islotes inflamatorias provocados por diferentes cepas de Helicobacter Pylori con atrofia glandular y metaplasia intestinal que son lesiones precancerosas.
Comienza en la región de la incisura angular luego se disemina en sentido proximal y distal.
Gastritis distintivas
Tuberculosis: su frecuencia ha aumentado a causa de la asociación con SIDA.
Hay compromiso piloroduodenal, con múltiples úlceras, engrosamiento de la pared gástrica y la obstrucción del tracto de salida pilórico.
El diagnostico especifico se basa en la demostración de granulomas caseosos en tejidos de biopsia y en cultivos positivos.
Sífilis: al igual que la TBC su frecuencia aumenta por la asociación con SIDA
El cuadro se asemeja al de la linitis gástrica ó el linfoma y por lo tanto se presenta con náuseas, vómitos ó saciedad temprana.
Citomegalovirus: se ve en pacientes inmunocomprometidos (SIDA- Trasplantados hepáticas y renales, etc.)
En el estómago el aspecto más llamativo son los pliegues gástricos engrosados en el antro o un proceso localizado o difuso en el cuerpo gástrico.
El citomegalovirus afecta capas más profundas de la mucosa, en las células endoteliales y las glándulas mucosas, a diferencia del Herpes Virus que las lesiones son superficiales.
Gastritis de Ménétrier: La gastritis de Ménétrier es una entidad rara, caracterizada por hipersecreción rica en proteínas y un cuadro de hipoalbuminemia, acompañado o no de edemas, ascitis y aun anasarca. El paciente no presenta signos de enfermedad renal, hepática o cardiaca, ingiere normalmente proteínas y no se encuentra la causa etiológica de su pérdida de albúmina. La radiografía seriada gastroduodenal con doble con doble contraste muestra pliegues gigantes, el estudio de la secreción gástrica revela hipoclorhidria, y en la biopsia gástrica se observa una gastritis crónica con tendencia a la atrofia.
El diagnostico se realizará utilizando albúmina marcada con I, su vida media estará notablemente acortada, menos de ocho días. La radiactividad en materia fecal mostrará un incremento llamativo. En el jugo gástrico se puede medir la radiactividad y realizar un proteinograma por electroforesis, en el cual se observará una banda típica de albúmina.
Gastritis hipertrófica hipersecretora: Se trata de un enfermo generalmente con antecedentes de úlcera gastroduodenal crónica intratable o de un gastrectomizado con úlceras recidivantes, o de un paciente afectado de diarrea crónica con esteatorrea. Presenta una marcada hipersecreción gástrica basal cuyo débito es similar o representa más de un 60% del débito posestímulo máximo. En estas circunstancias se debe pensar en un síndrome de Zollinger-Ellison, producido por un gastrinoma localizado en el páncreas o el duodeno; este tumor secreta altas concentraciones de gastrina y provoca la marcada hipersecreción gástrica basal y la ulcera intratable o la diarrea crónica. Frente a este diagnóstico presuntivo se debe efectuar un dosaje de gastrina por radioinmunoensayo y eventualmente una prueba de la secretina.
Gastropatía glandular hipersecretora: En esta rara entidad existe una marcada hipertrofia e hiperplasia glandular de etiología desconocida, que cursa con acentuada hiperclorhidria; el paciente suele ser portador de una úlcera duodenal intratable y la cirugía significa la curación de la enfermedad. La gastrinemia es normal.
Síntomas
La sintomatología es polimorfa, variable con vómitos alimenticios, biliosos, mucosos y en ocasiones hemorrágicos, que pueden estar o no precedidos por nauseas. La epigastralgia no tiene ritmo horario, ni diario ni periodicidad anual, el enfermo se siente mejor con el estómago vacío.
En la gastritis aguda al suprimir las causas desencadenantes, la sintomatología remite en pocos días.
Existen formas de presentación que pueden ser indicativas de gastritis
Hemorragia
Aclorhidria o Anemia Perniciosa
Ascitis, edemas, pliegues gástricos gigantes, hipoproteinemia con hipoalbuminemia (Enfermedad de Ménétrier)
En resumen, los intentos para establecer una correlación entre la gastritis y un cuadro sintomático especifico han fracasado.
Metodología de estudio
El diagnóstico de la gastritis es patrimonio de la biopsia y de su histopatológica, excepto en la hemorragia donde se establece por endoscopia.
La radiografía seriada gastroduodenal con doble contraste podrá mostrar
erosiones crónicas, bajo la forma de pequeñas imágenes lacunares redondeadas, que serán confirmadas por la fibroscopía; otras veces existirán pliegues gruesos gigantes, que plantearán el diagnostico diferencial entre una gastritis perdedora de proteínas tipo Ménétrier, un linfosarcoma gástrico, o un síndrome de Zollinger-Ellison. En la gastritis crónica tipo A de la anemia perniciosa, el radiólogo V. D´Allotto describió los siguientes signos: estomago tubular, techo gástrico calvo y lisura de la curvatura mayor gástrica, que no son patognomónicos, ya que los pliegues gástricos gruesos o finos dependen de la contracción de la muscularis mucosae.
El test de Kay mide la secreción gástrica máxima utilizando la histamina, con la cual son estimuladas el 100% de las células parietales. Esta prueba es la más reproducible y confiable. El débito normal es de 10 a 25 mEq/hora; en las gastritis generalmente el débito es normal, y tiene valor cuando es de cero o cercano al cero. Esto último es válido para el pepsinógeno plasmático o el uropepsinógeno, cuyos niveles tienen valor cuando son cercanos al cero e indican atrofia gástrica o anemia perniciosa.