Julio Libman y Astrid M. Libman
El síndrome de hiperplasia suprarrenal congénita, cuya expresión clínica varía según sus diversas formas, se debe a la deficiencia total o parcial de alguna de las enzimas que intervienen en la síntesis de los esteroides adrenales, con disminución de la producción de esteroides distales al bloqueo y aumento de algunos anteriores al mismo, por acumulación y desviación de la síntesis hacia vías metabó1icas alternas.
Fisiopatología
La hiperplasia suprarrenal congénita constituye un grupo de alteraciones autosómicas recesivas de la esteroidogénesis adrenal.
La síntesis de los esteroides suprarrenales se desarrolla a partir del colesterol por la acción de una serie de enzimas (fig. 66-1). Su producción y secreción, especialmente la de los glucocorticoides y los esteroides de acción sexual, y en mucha menor proporción la de aldosterona, es regulada por centros del SNC, que controlan la producción de la hormona hipotalámica liberadora de ACTH, péptido de 41 aminoácidos que, a través del sistema portal hipotálamo-hipofisario, alcanza la adenohipófisis, donde determina la liberación de ACTH, un péptido de 39 aminoácidos cuyo efecto fisiológico principal es el de estimular la síntesis de cortisol. La secreción de ACTH, que se produce en forma episódica, y la de cortisol, están sujetas a lo que se conoce como ritmo circadiano, con niveles máximos en horas de la mañana y mínimos en las últimas horas del día. En circunstancias normales, el cortisol inhibe la secreción de ACTH y de la hormona hipotalámica liberadora de ACTH, determinando lo que se conoce como un mecanismo de retroalimentación negativa.
El bloqueo de la síntesis de cortisol por falta total o parcial de alguna de las enzimas que intervienen en su síntesis, causa la disminución de sus niveles plasmáticos, aumento de la producción de ACTH e hiperplasia suprarrenal bilateral. Cuando la deficiencia enzimática es acentuada, no se normaliza la producción de cortisol, pero aumenta significativamente la de los precursores con acción androgénica o de retención de Na+, lo cual determina una serie de manifestaciones clínicas variables de acuerdo con la localización del bloqueo enzimático.
Síntomas y signos
Las manifestaciones del cuadro clínico varían de acuerdo con el déficit enzimático presente.
Deficiencia de 21-hidroxilasa. Es el tipo más común de hiperplasia suprarrenal congénita. Existen dos variedades: a) la forma simple y b) la forma perdedora de sal.
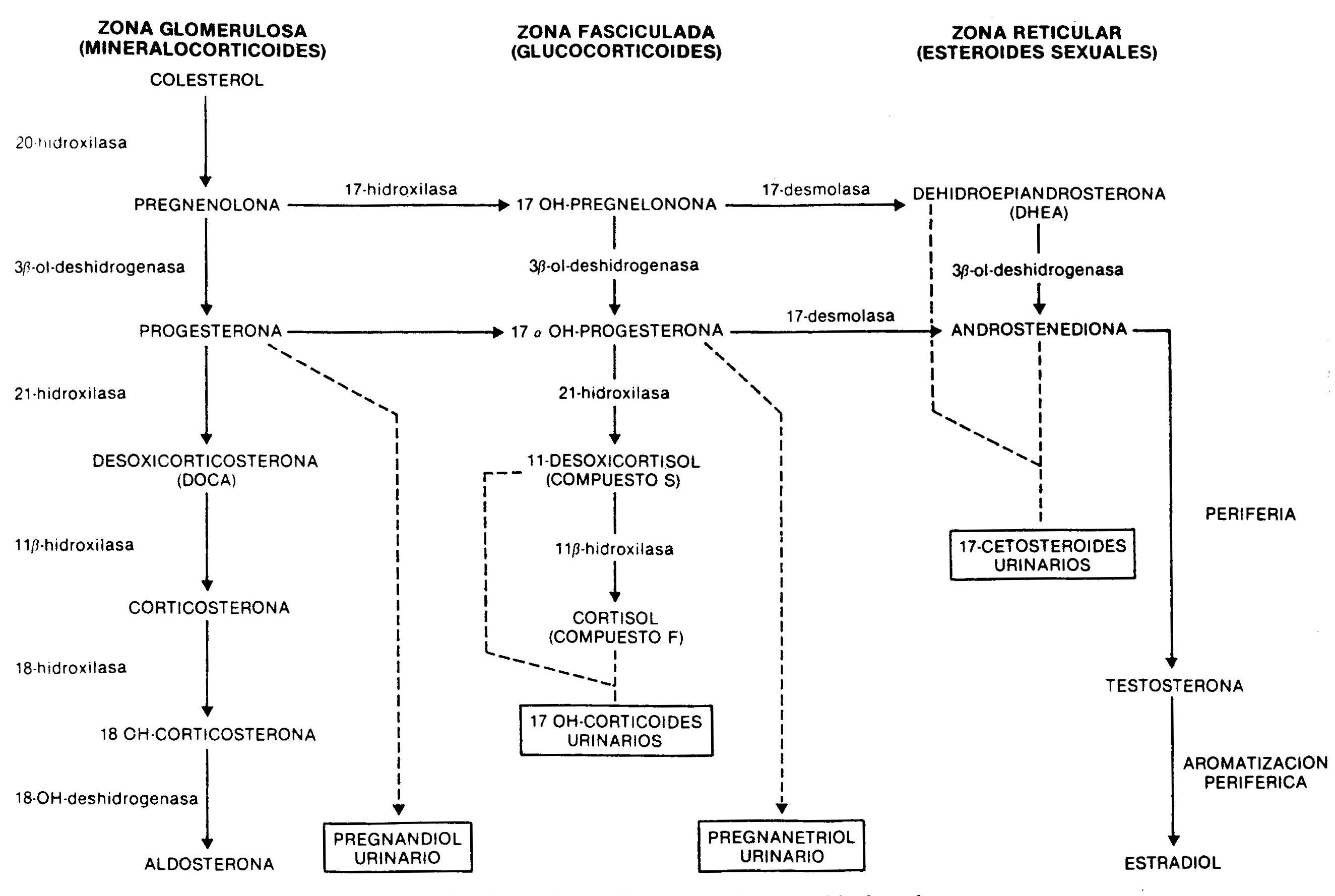
Fig. 66.1 – Síntesis de esteroides suprarrenales a partir del colesterol
a) En la variedad simple existe una deficiencia parcial bien compensada por un aumento de la ACTH, de manera que la producci6n de cortisol se aproxima a la normalidad. El incremento de la ACTH produce una marcada elevación de andrógenos y precursores del cortisol. La androstenediona, muy aumentada en sangre, es un andrógeno débil que se metaboliza periféricamente a testosterona; esto causa la masculinización de los genitales externos durante la vida fetal en la paciente genotípicamente femenina, con agrandamiento del clítoris y grados variables de fusión de los labios mayores, que puede llegar a simular un varón con criptorquidia e hipospadias. En los varones no hay anormalidades en los genitales externos al nacer. Posteriormente ocurre una virilización progresiva en ambos sexos, con aparición de vello axilar y pubiano, facial, cambios en la voz y aumento de las masas musculares. Aun cuando en la primera infancia presentan una estatura mayor que la correspondiente a la edad y sexo, la fusión precoz de las epífisis por acción androgénica lleva a una estatura final baja. En la pubertad, y en ausencia de un tratamiento adecuado, no se produce el aumento fisiológico de las gonadotrofinas debido a una inhibición por los esteroides sexuales circulantes, y el resultado de esto es una amenorrea primaria en la mujer y testículos pequeños en el varón. En la forma simple, no perdedora de sal, no existen dificultades en el balance hidrosalino y la presión arterial es normal. Los 17-cetosteroides, la 17OH-progesterona y en menor grado el pregnandiol se encuentran aumentados, disminuyendo sus valores en orina a continuación de la administración durante 7 días de 1,25 mg diarios de dexametasona por m2 de superficie corporal.
b) En la forma perdedora de sal existe una deficiencia completa de 21-hidroxilasa. Aun cuando hay un incremento compensador de ACTH, los niveles de cortisol son bajos, al igual que los de aldosterona, de modo que los signos de insuficiencia suprarrenal aguda aparecen en el curso de la primera semana de vida, con anorexia, vómitos, pérdida de peso, diarreas, deshidratación e hiperkalemia. De no tratarse, se desarrolla un colapso vascular y sobreviene la muerte.
El diagnóstico prenatal de la deficiencia de 21-hidroxilasa puede realizarse en el primer trimestre del embarazo mediante el análisis genético molecular de las células de las vellosidades coriales y la cuantificación de 17-hidroxiprogesterona en una pequeña cantidad de líquido amniótico.
Deficiencia de 11-beta-hidroxilasa. Causa una deficiencia en la síntesis de cortisol con hipersecreción de ACTH. La altura del bloqueo determina la excesiva producción de precursores del cortisol, tales como el 11-desoxicortisol y su metabolito tetrahidroderivado que son cuantificados en la orina como 17OH-corticoides. Por consiguiente, éstos se encuentran elevados, al igual que la 17OH- progesterona y su metabolito, el pregnanetriol. La deficiencia limita también la conversión de desoxicorticosterona a corticosterona, con la consiguiente acumulación de este potente mineralocorticoide, responsable de la hipertensión arterial que se observa en esta forma de hiperplasia suprarrenal congénita. Como consecuencia del déficit enzimático, se produce igualmente el cortocircuito hacia la síntesis de andrógenos. La deficiencia de 11-hidroxilasa se caracteriza, en consecuencia, por virilización, hipertensión, aumento de los 17-ceto y 17- hidroxicorticoides urinarios y del 11-desoxicortisol plasmático y sus metabolitos urinarios.
Deficiencia de la 20-hidroxilasa o colesterol desmolasa. Es una forma poco común que afecta la conversión de colesterol a pregnenolona; por consiguiente, existe una alteración en la producción de glucocorticoides, mineralocorticoides y esteroides sexuales. La carencia de los primeros determina un cuadro grave de insuficiencia suprarrenal, con pérdida de Na+, deshidratación, hipovolemia e hipotensión. La deficiencia androgénica es causa de que los pacientes afectados tengan genitales externos femeninos, ya sea que su cariotipo sea XX o XY.
Deficiencia de 3-beta-ol-deshidrogenasa. Existe un defecto en la conversión de pregnenolona a progesterona, de 17OH-pregnenolona a 17OH-progesterona y de dehidroepiandrosterona a androstenediona. Como consecuencia se produce una disminución de mineralocorticoides, glucocorticoides y testosterona, lo cual causa insuficiencia suprarrenal con genitales ambiguos en los varones y moderada hipertrofia de clítoris en las mujeres, debidos a la acumulación de la dehidroepiandrosterona, un andrógeno débil. Este defecto también se encuentra presente en la gónada.
Deficiencia de 17-hidroxilasa. Este déficit enzimático da como resultado la incapacidad total o parcial para sintetizar cortisol y esteroides sexuales. Como se ve en la figura 66-1, esta enzima no está involucrada en la producción de mineralocorticoides. La producción de desoxicorticosterona, controlada por la ACTH, está muy aumentada, dando como resultado una discreta hipertensión arterial, retención de Na+, expansión del volumen plasmático e inhibición del sistema renina-angiotensina. La mayor producción de corticosterona compensa la menor síntesis de cortisol. Los varones muestran genitales ambiguos por producción disminuida de testosterona. La deficiencia enzimática se halla presente también en los ovarios, con la consiguiente falta de desarrollo sexual en la pubertad.
Metodología de estudio
De lo expuesto se infiere que cabe sospechar la existencia de una hiperplasia suprarrenal congénita en un recién nacido con genitales externos ambiguos, asociados o no a un cuadro de vómitos, deshidratación y colapso circulatorio, o bien al desarrollo de hipertensión. En un varón de mayor edad puede presentarse con crecimiento acelerado y pseudopubertad precoz, es decir, desarrollo de los caracteres sexuales secundarios con testículos infantiles.
En presencia de algunas de estas manifestaciones se debe evaluar la cromatina nuclear en un extendido celular de la mucosa bucal y en los leucocitos circulantes con el fin de determinar el sexo cromosómico, y cuantificar los 17-cetosteroides, 17OH-corticoides y pregnanetriol urinarios, y la 17OH-progesterona y el ionograma en sangre, junto con el 11-desoxicortisol, en caso de hipertensión concomitante. La edad ósea se encuentra avanzada en las placas radiográficas de mano y muñeca.